人为什么会衰老?一种理论认为,衰老的背后是表观遗传变异的累积。随着年龄增长,表观遗传发生的变化可能让细胞发生基因读取错误,导致衰老。其中一种重要变化就是DNA甲基化,即甲基分子在DNA上聚集,让本来应该打开的基因被关闭,或者相反。因此有人猜测,如果适当擦除一些甲基化,是不是可以逆转细胞的衰老?

逆转衰老,神经再生首次被证实
近日,哈佛医学院David Sinclair团队在顶级期刊《自然》上以封面报道形式发表的研究成果,支持了以上观点。科学家们选择了视网膜中的神经节细胞(RGC)作为目标,利用三种基因,让其实现“返老还童”,重新获得修复损伤和再生的能力。
论文的第一作者是吕垣澄博士,通讯作者是全球抗衰老研究的领军人物David Sinclair,哈佛医学院的何志刚、Bruce R. Ksander和Meredith S. Gregory-Ksander共同指导了本研究。提到科学家利用的三种基因,山中因子(OCT4、SOX2、KLF4和MYC)是个绕不开的工具。
山中因子与OSK
早有研究表明,山中因子的异位表达可以将培养的体细胞重新编程成为多能干细胞,这种方法甚至可以抹去细胞身份,重置DNA甲基化年龄。然而,山中因子抗衰老的能力,不是逆转衰老,而是直接将细胞“打回娘胎”。同时山中因子的这种超能力,会诱发畸胎瘤,甚至是在几天内导致实验动物死亡。因此,要想研究逆转衰老的问题,就有必要改变一下山中因子。
Sinclair团队剔除了Myc(癌基因的表达),保留了OCT4、SOX2和KLF4(OSK)。初步分析发现,OSK表达5天之后,就让mRNA谱变得年轻化了,最关键的是,细胞的原始身份还在。
OSK实验,显示出强大的再生能力
鉴于中枢神经系统是哺乳动物最先失去再生潜能的系统之一,Sinclair团队的研究人员选择了视网膜神经节细胞(RGCs)。科学家OSK送入小鼠的视网膜,然后通过药物控制三个基因的打开或关闭。
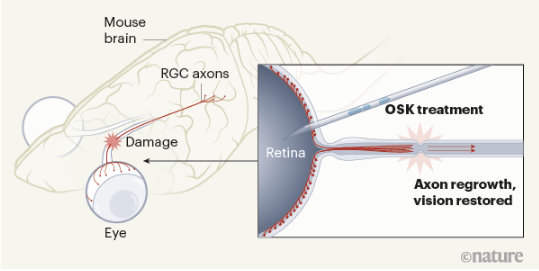
令人欣喜的是,当研究人员尝试将OSK递送到成年小鼠的视网膜RGC时,发现这些成熟的神经细胞显示出强大的再生能力,就像回到了发育早期。这些细胞在受伤后依然还能再长出新的轴突。
为了排除年轻小鼠视网膜神经节细胞残余自然再生能力对研究结果的干扰,Sinclair团队成员又在老年小鼠身上做了同样的研究。在12个月大的老龄小鼠中,OSK治疗使视网膜神经节细胞的存活率翻倍,效果与在1个月和3个月大的小鼠中观察到的结果相似。
在青光眼模型中,与治疗前相比,OSK治疗后的小鼠视力有了显著的提高。据了解,这也是第一次逆转青光眼对视力的损伤。
逆龄时代已来
在《自然》同期发表的评论文章中,斯坦福大学医学院的Andrew D. Huberman博士探讨了这种“逆龄”方法应用于人类的潜力。

他指出,三种转录因子对人的作用还有待进一步验证,但鉴于RGC是真正的大脑神经元,我们有充分的理由认为三种因子对大脑、脊髓部位的其他神经元可以产生同样的显著作用。
“这项工作首次证实,我们有可能对视神经这样的复杂组织进行安全的重编程,使其变得年轻。”研究机构的新闻稿指出,“作为概念验证,这种方法也为治疗各种与衰老相关的人类疾病奠定了基础。”我们相信,这一发现有望促进各种器官的组织修复,并扭转人类衰老和年龄相关疾病。